01 制药用水中注射用水定义介绍
01 制药用水中注射用水定义介绍
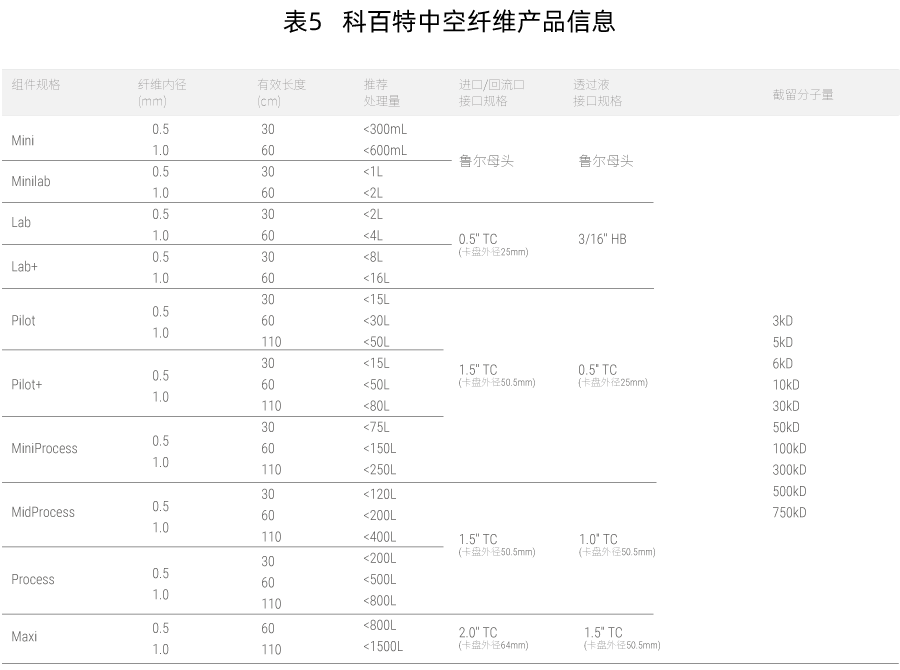
水是药物生产中用量大、使用广的一种辅料,在原料生产、分离纯化、制剂生产、设备清洗等整个制药生产工艺过程中都有应用。制药用水的质量会直接影响药物制剂质量,从而影响患者生命安全,因此,各国药典对于制药用水及注射用水均有明确的要求和规定,具体见下表1。
02 注射用水制备方法对比
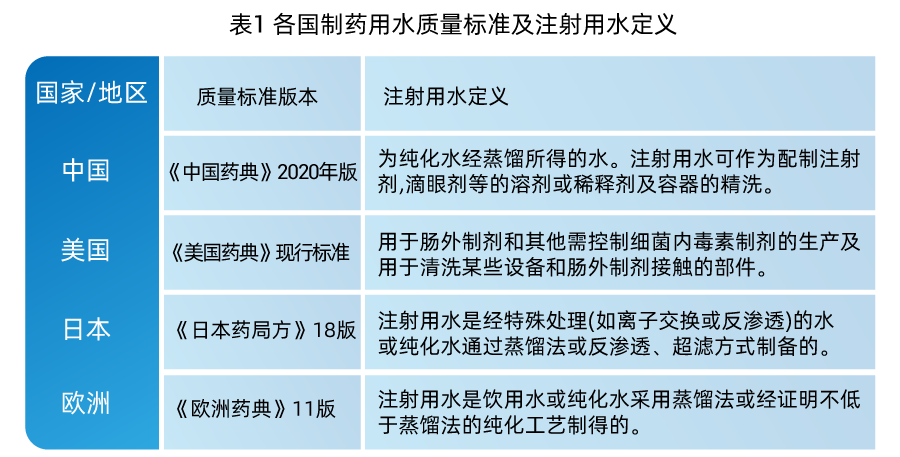
各国家均会使用蒸馏法来制备注射用水,如下表2所示。其中欧洲药典在2017年进行了关于注射用水专篇0169的修订,这对注射用水的生产带来一场变革。自实施起,欧盟开始允许使用等同于蒸馏技术的方法来生产注射用水,例如,利用膜分离反渗透法、结合超滤步骤的电去离子技术等。WHO TR 1025附件3《非蒸馏法制备注射用水》也指出,注射用水的制备通过蒸馏作为最后的步骤,也可以通过蒸馏以外的方法制备,如去离子、电去离子、纳滤、超滤、软化、除锈、初滤和脱气、紫外线处理等,连同其他技术,也可考虑与单道或双道 RO 结合使用。当前,欧洲、美国、日本都允许饮用水直接以蒸馏或非蒸馏方式制备注射用水。
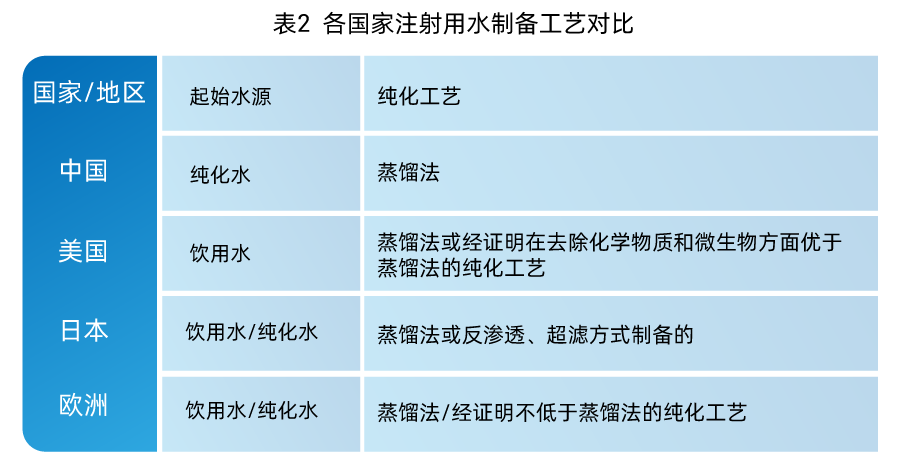
而欧洲、美国、日本都允许饮用水直接以蒸馏或非蒸馏的方式制备注射用水。相比较蒸馏法而言,非蒸馏法有利于提高原水利用率、节能减排、经济环保,近年来在欧洲、美国、日本得到广泛推广。但非蒸馏法在常温下进行,对于制备过程水中的微生物和细菌内毒素控制要求更高,因此,结合国情特点,我国还是仅允许蒸馏法制备注射用水。
03 非蒸馏法制备注射用水(膜分离技术)

 2025年版《中国药典》通则0261对注射用水的定义重新进行了修订,指出注射用水为纯化水经蒸馏所得,或为通过一个等同于蒸馏的纯化工艺制备所得。
2025年版《中国药典》通则0261对注射用水的定义重新进行了修订,指出注射用水为纯化水经蒸馏所得,或为通过一个等同于蒸馏的纯化工艺制备所得。此前《欧洲药典》设置高纯水这一类别,允许以非蒸馏的方式(如采用反渗透技术与超滤/去离子等技术相结合的方法)制备高纯水,使用范围规定:当系统中无须采用注射用水进行配制,但其对于水中微生物指标有严格控制时使用。在积累多年实践经验之后,欧盟于2017 年生效了非蒸馏方法用于制备注射用水相关条例,例如:利用膜分离反渗透法,结合超滤步骤的电去离子技术等。自此,高纯水退出历史舞台。随着近年来行业内装备设施和技术水平的发展,我国亦可考虑通过设立高纯水作为过渡,逐步放开注射用水的净水工艺,与国际接轨。

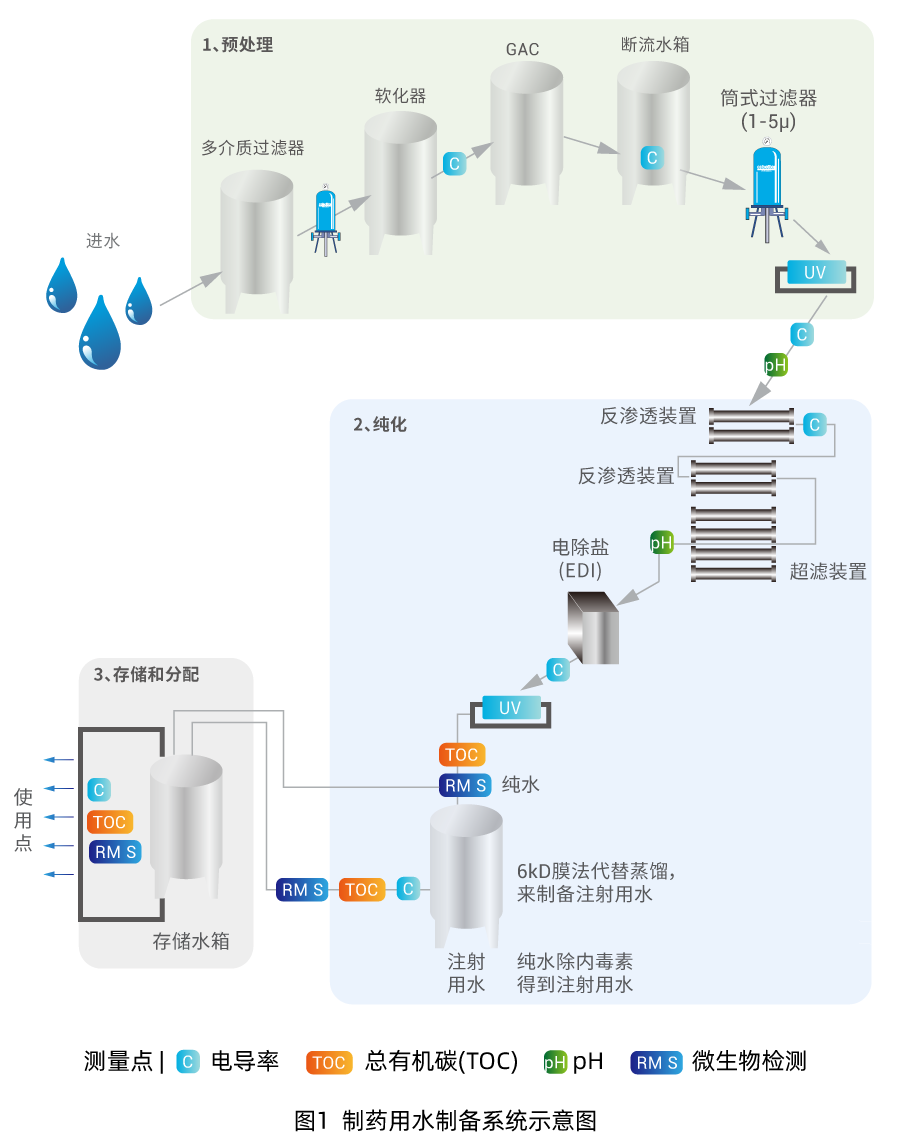
04 科百特6kD中空拦截内毒素效果
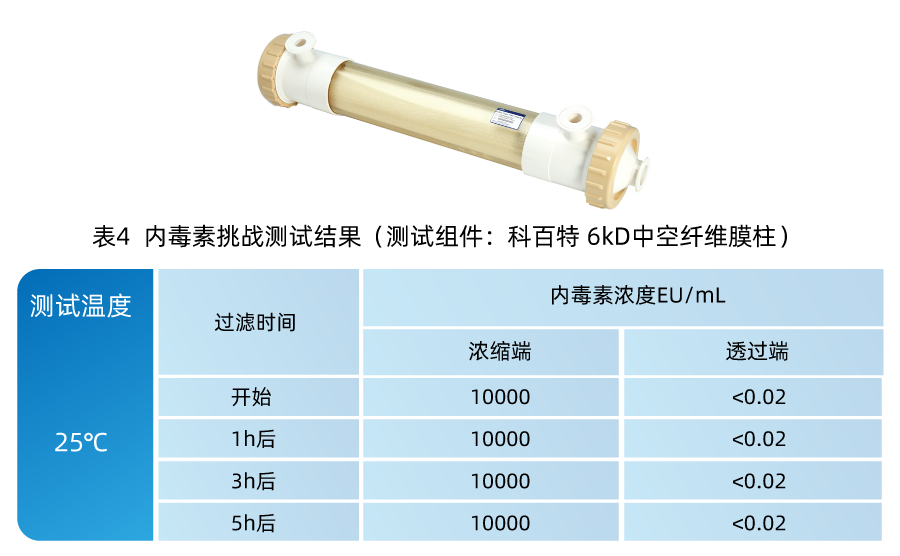
如表4所示,使用科百特 6kD中空纤维膜柱对10000EU/mL的内毒素挑战液进行超滤,取透过端溶液检测内毒素浓度<0.02 EU/mL,初步判断可满足注射用水中对内毒素<0.25EU/mL的标准。结合2025年版《中国药典》通则0261对注射用水的定义进行重新修订,这为使用非蒸馏法——如膜法制备注射用水带来了可能。