近期,FDA对中国某分析机构发出警告信,直指其数据记录不完整、不能有效追溯,电子数据存储及访问存在修改、删除等风险,质量体系监管缺失等质量体系管理漏洞。这一事件再次为行业敲响警钟:实验室质量管理不仅关乎合规性,更是企业信誉的生命线与客户信任的基石。
科百特应用验证实验中心(简称:AVL),创立于2007年,致力于服务全球医药公司的过滤验证及应用技术分析。目前已累计为全球1500多家医药客户提供超35000份过滤验证报告,并协助客户完成注册申报或一致性评价工作。面对行业痛点,科百特AVL是如何构建牢不可破的质量体系的呢?下面结合FDA警示,深度解析其质量管理体系的“硬核实力”。
以 ISO 17025 和 GMP 为框架,从“五大维度”构建质量防线:

数据管理“铁三角”护航数据完整性
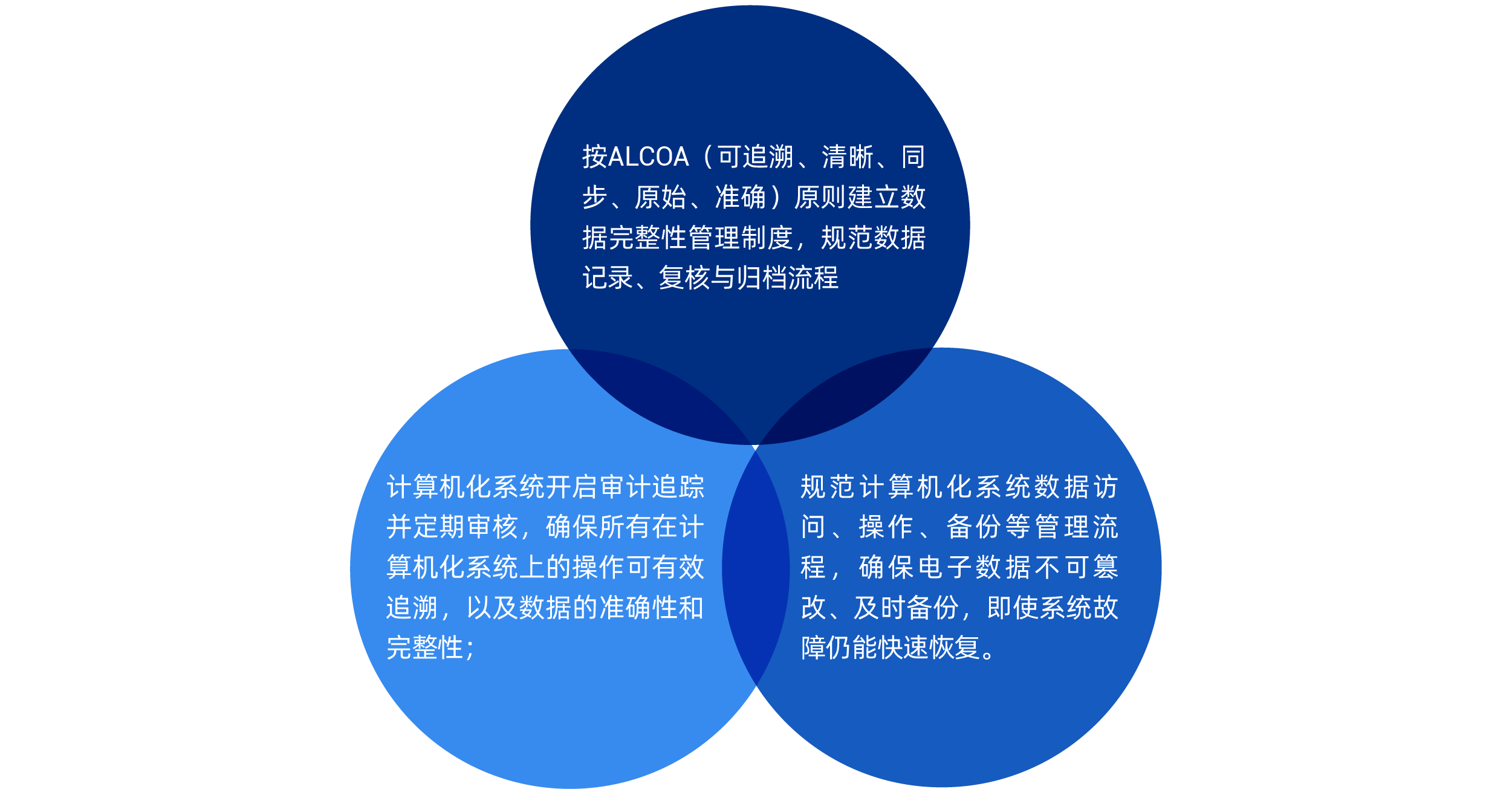
质量管理“双保险” 确保质量体系监管到位
· 20多位质量管理人员 + 100多位制药经验的工程师,组成兼具GMP合规意识与技术执行力的“黄金团队”
· 每年接受300余家全球药企的现场审计,同步执行内审与管理评审,确保体系动态合规。
行业启示:质量体系如何“防患于未然”?
技术为基
善用数字化工具、强化数据管理;
人才为本
建立常态化培训机制,提升全员质量意识;
合规为纲
以ISO、GMP等质量体系标准为框架,动态内审与外审结合,实现体系与国际标准同步进化。
FDA的警告信不是终点,而是质量升级的起点,唯有将质量管理内化为企业基因,才能在合规与创新中持续领跑。科百特AVL也将持续升级质量管理体系,继续为您提供优质的验证及应用服务!




